2025年成考高起点《理化综合》每日一练试题09月16日
2025-09-16 12:01:39 来源:勒克斯教育网
2025年成考高起点《理化综合》每日一练试题09月16日,可以帮助我们积累知识点和做题经验,进而提升做题速度。通过成考高起点每日一练的积累,助力我们更容易取得最后的成功。
单选题
1、有Xn+、Yn+、Z三种微粒,其电子层结构相同,下列分析中正确的是()。
- A:微粒半径大小:Xn+>Yn+
- B:Z不一定是稀有气体元素
- C:原子序数:Z>Y>X
- D:原子半径关系:X
答 案:A
2、一定条件下在密闭容器中合成氨的反应: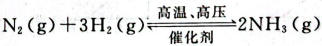 (放热反应),下列说法正确的是
(放热反应),下列说法正确的是
- A:
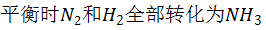
- B:升高温度平衡正向移动
- C:

- D:催化剂可以加快反应速率
答 案:D
解 析:A选项,此反应为可逆反应,即同条件、同时向正逆两个方向进行的反应,反应物与生成物同时存在;B选项,此反应为放热反应,升高温度,平衡向吸热方向移动,即逆方向;C选项,减小压强,会向气体分子总数增大的方向移动,即逆方向移动,不会让N2的转化率增加;D选项,适当的催化剂,可增大其化学反应速率,故D选项正确。
多选题
1、某溶液中有NH4+、Mg2+、Al3+、Fe2+等4种离子, 若向其中加入过量的 NaOH溶液, 微热并搅拌, 再加入过量的盐酸, 溶液中大量减少的阳离子是
- A:NH4+
- B:Mg2+
- C:Fe2+
- D:Al3+
答 案:AC
主观题
1、如图,水平面内有两条相距L的平行金属导轨,导轨足够长,其左端接有一阻值为R的电阻,导体棒ab放置在导轨上。空间存在垂直于导轨所在平面的匀强磁场,磁感应强度大小为B。现使ab以恒定速度v沿导轨向右运动,运动过程中ab始终与导轨垂直并接触良好。不计导轨和导体棒的电阻。求(1)导体棒ab所受安培力的大小;(2)电阻R上消耗的功率。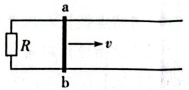
答 案:
解 析:
2、实验室选用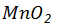 与10mol/L浓盐酸反应制备氯气,其化学反应方程式是 ,
与10mol/L浓盐酸反应制备氯气,其化学反应方程式是 ,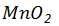 在反应中作 (填“氧化剂”或“还原剂”);若生成标准状况下氯气2.8L,反应中转移电子多少摩尔?消耗该盐酸溶液多少毫升?
在反应中作 (填“氧化剂”或“还原剂”);若生成标准状况下氯气2.8L,反应中转移电子多少摩尔?消耗该盐酸溶液多少毫升?
答 案:
解 析:
填空题
1、FeCl3溶液中先通入过量的SO2,再滴加BaCl2溶液,产生的白色沉淀为()(填化学式),说明SO,具有()性。
答 案:BaSO₄;还原
解 析:本题考查了二氧化硫的性质的知识点。 二氧化硫具有还原性,能与氧化铁发生氧化还原反应生成硫酸根,可用氯化钡检验生成的硫酸根。
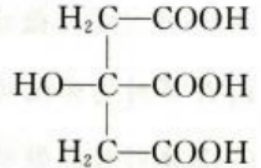
2、元素X、Y、Z都位于短周期,它们的原子序数按X、Y、Z的顺序依次减小。X原子的最外层与最内层电子数之比为1:1,Z原子的最外层电子数是内层电子数的2倍,Y原子的核外电子数比Z原子的多2个。化合物XY的化学键为()键,化合物ZY,的电子式为()
答 案:离子;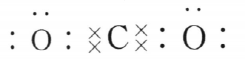
解 析:根据核外电子排布和元素周期表可推断出元素X为Mg,Y为O,Z为C,故MgO中含离子键,CO2的电子式为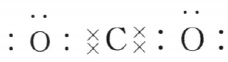
简答题
1、图6—24是弹簧振子的振动图像,试回答下列问题: (1)振动的振幅、周期、频率各是多少?
(2)如果从0点算起,到图线上哪一点为止振子完成了一次全振动?从A点算起呢?
(3)从0到1.6s时间内,哪些点的动能最大?哪些点的势能最大? 
答 案:(1)2cm,0.8s,1.25Hz(2)D点,E点 (3)O、B、D、F、H点的动能最大,A、C、E、G点的势能最大
2、用纯净的氯酸钾和二氧化锰混合物7.56g制取氧气,加热至不再有氧气放出为止,冷却后残留在容器里的固体物质为5.32g。问: (1)反应产生的氧气在标准状况下的体积为多少升?
(2)原混合物中有氢酸钾多少克?
答 案:按题意知,反应生成O2的质量为7.56g~5.32g=2.24g 2.24gO2占的体积为(标准状况)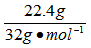 ×22.4L﹒mol-1=1.568L
×22.4L﹒mol-1=1.568L
设原合物中KClO3的质量为xg,根据反应的化学方程式 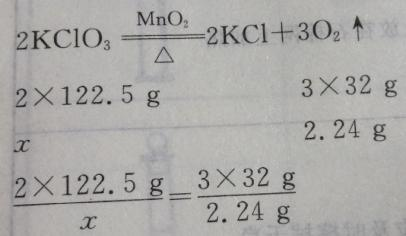 解得x=5.72g
解得x=5.72g
答:产生的O2在标准状况下的体积为1.568L,原混合物中含KClO35.72g。



