2025年成考高起点《理化综合》每日一练试题08月25日
2025-08-25 12:13:24 来源:勒克斯教育网
2025年成考高起点《理化综合》每日一练试题08月25日,可以帮助我们积累知识点和做题经验,进而提升做题速度。通过成考高起点每日一练的积累,助力我们更容易取得最后的成功。
单选题
1、下列说法正确的是()
- A:天然气的主要成分是正丁烷
- B:84消毒液的有效成分是氯化钠
- C:花生油的主要成分是软脂酸
- D:石灰石的主要成分是碳酸钙
答 案:D
解 析:熟记常见物质的成分,能正确判断主要成分和有效成分,如天然气的主要成分是甲烷、84消毒液的有效成分是次氯酸钠、花生油的主要成分是不饱和脂肪酸、石灰石的主要成分是碳酸钙。
2、电动势为3V的电池,在电路中输出3A的电流,由此可知()。
- A:内外电阻相差1Ω
- B:内外电阻之和为1+Ω
- C:外电阻为1Ω
- D:内电阻为1Ω
答 案:B
多选题
1、某溶液中有NH4+、Mg2+、Al3+、Fe2+等4种离子, 若向其中加入过量的 NaOH溶液, 微热并搅拌, 再加入过量的盐酸, 溶液中大量减少的阳离子是
- A:NH4+
- B:Mg2+
- C:Fe2+
- D:Al3+
答 案:AC
主观题
1、如图,一质量为m1的木块静置在光滑的水平面上,一质量为m2的子弹以速度v0水平射入木块,进入木块s距离后相对木块静止。设子弹相对木块静止前受到的阻力恒定。求从子弹开始进入到相对木块静止这段时间内
(1)子弹与木块组成的系统损失的机械能。
(2)木块移动的距离。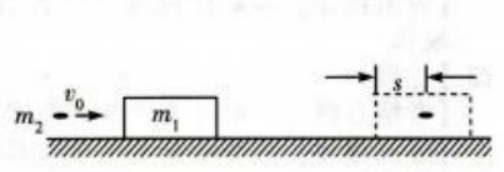
答 案:(1)根据动量守恒定律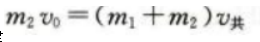 根据功能关系
根据功能关系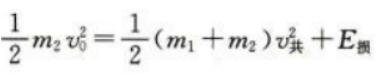
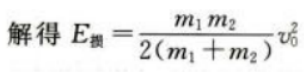 (2)设子弹与木块间摩擦力为f,则E损=fs设物块运动距离为L,对物块运用动能定理
(2)设子弹与木块间摩擦力为f,则E损=fs设物块运动距离为L,对物块运用动能定理
2、工业上用焙烧NaHCO3的方法生产纯碱(Na2CO3)。现有17.5g的NaHCO3样品,加热分解完全后,生成标准状况下的CO2气体2.24L。写出NaHCO3分解反应的化学方程式,计算此NaHCO3样品的纯度。
答 案:NaHCO3分解反应的化学方程式如下: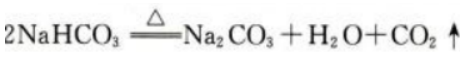 反应生成标准状况下的CO2气体2.24L,其物质的量为0.1mol,故加热完全分解的NaHCO3的物质的量为0.2mol,质量为16.8g,此NaHCO3样品的质量为17.5g,所以此NaHCO3样品的纯度为16.8g/17.5g×100%=96%。
反应生成标准状况下的CO2气体2.24L,其物质的量为0.1mol,故加热完全分解的NaHCO3的物质的量为0.2mol,质量为16.8g,此NaHCO3样品的质量为17.5g,所以此NaHCO3样品的纯度为16.8g/17.5g×100%=96%。
填空题
1、氨气和氧气在催化剂存在的条件下反应生成一氧化氮和水时,若有10mol电子发生转移,则生成的一氧化氮为()mol。
答 案:2
解 析:氧化还原反应中得失电子总数相等,生成一氧化氮时,氮元素的化合价从-3升高到+2,每生产1molNO,转移5mol电子,故有10mol电子发生转移时,生成的NO为2mol。
2、氯化铝溶液滴入烧碱溶液中发生反应的离子方程式为()
答 案: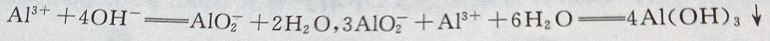
解 析: 溶液滴入烧碱溶液,开始时碱过量,两者发生反应为
溶液滴入烧碱溶液,开始时碱过量,两者发生反应为
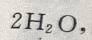 随着
随着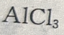 的加入,生成的
的加入,生成的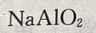 又会与过量的
又会与过量的 溶液反应,
溶液反应,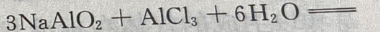

简答题
1、飞机在h=500m高空中以υ1=60m/s的速度水平飞行.海面上有一艘敌舰以υ2=15m/s的速度与飞机同向航行.该飞机要轰炸敌舰,应在何处投弹?如果敌舰与飞机反向航行,其他条件不变,应在何处投弹?(g取10m/s2)
答 案:炸弹脱离飞机后做平抛运动,初速度就是飞机的速度υ
2、如图1—15所示,两根轻质细杆AC、BC用铰链固定在墙上构成一个直角三角形支架,在C处挂一盏吊灯。已知AC=1.2m,BC=2m,吊灯重200N。求杆AC和BC所受力的大小和方向。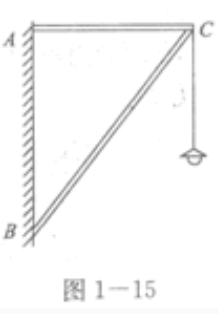
答 案:取C点为研究对象,分析其受力情况:绳子的拉力FT=G,AC杆的拉力FNl和BC杆的支持力 



