2025年成考高起点《理化综合》每日一练试题07月17日
2025-07-17 12:11:36 来源:勒克斯教育网
2025年成考高起点《理化综合》每日一练试题07月17日,可以帮助我们积累知识点和做题经验,进而提升做题速度。通过成考高起点每日一练的积累,助力我们更容易取得最后的成功。
单选题
1、如图3—5所示,在沿水平向右运动的车厢内,用绳昂起一个质量为m的小球。当悬线向后倾斜,与竖直方向间的夹角为θ时,则车前进的加速度是()。 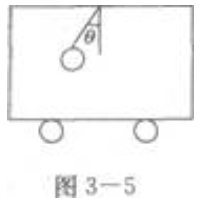
- A:gsinθ
- B:gcosθ
- C:gtanθ
- D:gcotθ
答 案:C
2、根据元素周期律,下列性质比较中,错误的是
- A:非金属性:
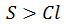
- B:稳定性:
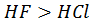
- C:酸性:
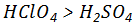
- D:碱性:
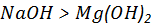
答 案:A
解 析:同周期从左向右非金属性增强,则非金属性:Cl>S,故应选A选项。
多选题
1、某溶液中有NH4+、Mg2+、Al3+、Fe2+等4种离子, 若向其中加入过量的 NaOH溶液, 微热并搅拌, 再加入过量的盐酸, 溶液中大量减少的阳离子是
- A:NH4+
- B:Mg2+
- C:Fe2+
- D:Al3+
答 案:AC
主观题
1、一绝缘细绳上端固定,下端连接在一质量m=0.08kg、长度l=0.4m的均匀金属棒中心,整个装置处在一匀强磁场中,磁场的磁感应强度大小B=0.5T,方向竖直向上,如图所示。现使一电流流过金属棒,已知电流大小I=3A,方向垂直于纸面向里,重力加速度大小g取10m/s2。求
(1)金属棒所受安培力的大小和方向。
(2)平衡后细绳中张力的大小及细绳与竖直方向夹角的正切值。
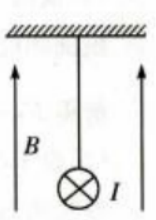
答 案:.(1)金属棒所受安培力为F=BIL=0.6N,根据左手定则知,方向水平向右。 (2)金属棒所受重力为G=mg=0.8N平衡后,安培力与重力的合力与绳中张力等大反向,设细绳与竖直方向的夹角为θ,则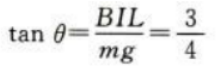 绳中张力大小为
绳中张力大小为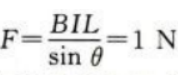
2、实验室选用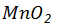 与10mol/L浓盐酸反应制备氯气,其化学反应方程式是 ,
与10mol/L浓盐酸反应制备氯气,其化学反应方程式是 ,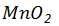 在反应中作 (填“氧化剂”或“还原剂”);若生成标准状况下氯气2.8L,反应中转移电子多少摩尔?消耗该盐酸溶液多少毫升?
在反应中作 (填“氧化剂”或“还原剂”);若生成标准状况下氯气2.8L,反应中转移电子多少摩尔?消耗该盐酸溶液多少毫升?
答 案:
解 析:
填空题
1、在淀粉加稀硫酸水解后的溶液中,为证明淀粉已发生水解,可先加入一定量的______,然后再加入______加热,如有银镜出现说明已经水解,为证明淀粉并没有完全水解,可加入______,出现______现象。
答 案:碱溶液;银氨溶液;碘水;蓝色
2、A、B两元素的离子具有相同的电子数,A、B两元素的单质都能与水剧烈反应,在反应中A单质作还原剂,B单质作氧化剂。A与B反应的生成物的电子式为()。
答 案:
解 析:根据题给条件知:在反应中A单质作还原剂则为金属元素,B单质作氧化剂则为非金属。而非金属单质常温下能与水剧烈反应的只有F2,其阴离子为2、8结构。
简答题
1、Na2CO3·l0H2O放在敞口容器内会逐渐变成粉末,这现象称为(),而NaOH固体放置时表面会形成溶液,这现象称为().
答 案:风化;潮解
2、1体积水(密度为1g/cm)吸收了560体积(标准状况下)氨气,所得氨水的密度为0.90g/cm,求此溶液中溶质的质量分数。用此氨水10mL与含7.74gH3PO4的溶液混合,恰好完全反应,求此反应生成盐的分子式。
答 案:(1)设水的体积为1L,1L水吸收NH3的质量为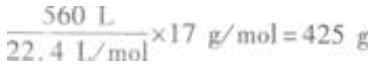 氨水中NH3的质量分数为
氨水中NH3的质量分数为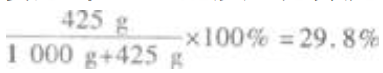 (2)10mL氨水中含NH3的物质的量为
(2)10mL氨水中含NH3的物质的量为 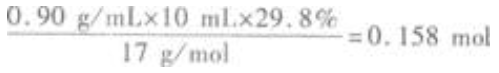 H3PO4的物质的量为
H3PO4的物质的量为 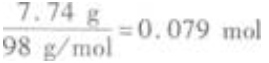 NH3与H3PO4的物质的量之比为
NH3与H3PO4的物质的量之比为 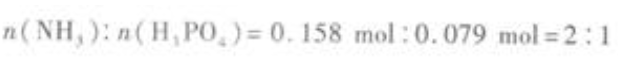 反应方程式为
反应方程式为  生成盐的分子式为(NH4)2HPO4。 (1)解此题首先应把体积单位具体化。设其为“L”,变为“1L水溶解560L(标准状况下)NH3”,这样便于计算。 (2)因NH3与H3PO4反应,可能有三种产物:NH4H2PO4、(NH4)2HPO4和(NH4)3PO4,所以应知道n(NH3)与n(H3PO4)的比值,才能知道生成盐的分子式。
生成盐的分子式为(NH4)2HPO4。 (1)解此题首先应把体积单位具体化。设其为“L”,变为“1L水溶解560L(标准状况下)NH3”,这样便于计算。 (2)因NH3与H3PO4反应,可能有三种产物:NH4H2PO4、(NH4)2HPO4和(NH4)3PO4,所以应知道n(NH3)与n(H3PO4)的比值,才能知道生成盐的分子式。



